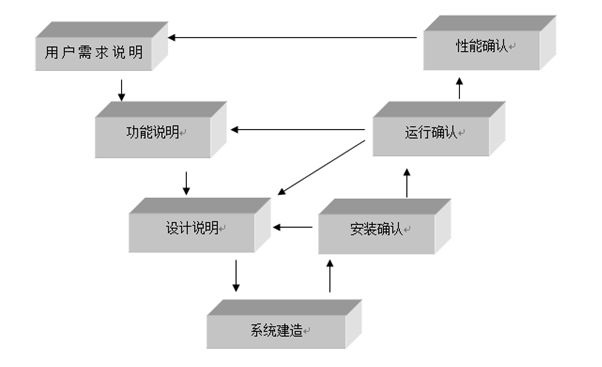
根据《医疗器械注册管理办法》,建立质量管理体系是产品注册的基本要求。而验证和确认又往往是体系核查的重中之重,特别是无菌医疗器械。
无菌医疗器械因其直接或间接与人体血液或肌体相接触的特殊性,决定了必须对其从生产场地到生产环节等的严格要求和控制。因此,为了保证生产场地和生产环节等符合无菌医疗器械的要求,在一些环节需要进行验证和确认。证标客根据《医疗器械生产质量管理规范》,把无菌医疗器械生产企业所需的验证和确认项目整理如下。
一、机构和人员
1. 人员净化效果(手消毒)验证
2. 人手及产品初始菌验证
3. 洁净工作服清洗效果验证
4. 消毒剂消毒效果验证
二、厂房和设施
5. 洁净室最大容纳人数验证
6. 洁净室环境验证
7. 洁净室消毒验证
8. 制水系统验证
9. 压缩空气系统验证
三、设备
10. 关键生产及检测设备的验证
11. 设备工装工具的清洁验证
四、设计开发
12. 产品的设计验证、确认及设计转换的确认
五、生产管理
13. 无菌包装封口过程确认
14. 产品、物料和自配试剂的有效期验证
15. 对关键过程的验证和特殊过程的确认
16. 清场及消毒的验证
17. 物料及产品清洗的验证
六、质量控制
18. 物料及产品初始污染菌和微粒污染验证
19. 产品初始菌和微粒污染验证及其检测方法的验证
20. 无菌检验方法验证
21. 微生物限度检验方法验证
22. 环氧乙烷灭菌过程确认及使用软件的确认
杭州证标客医药技术咨询有限公司位于中国杭州,是医疗器械专业服务第三方。为广大客户提供医疗器械法律法规、经营开办、医疗器械生产质量管理体系、医疗器械注册、临床试验、CRC、CE、FDA、医疗信息系统定制开发一站式服务,是江浙沪地区极少数有医疗器械全流程服务能力的机构之一。如有任何需求,请随时联系叶工18058734169。
无菌医械生