截止2024年2月,我国已有387项医疗器械原材料或关键部件完成医疗器械主文档登记,医疗器械主文档内容主要涉及医疗器械的原材料和某些关键部件,而不是成品的医疗器械。我国推动医疗器械主文档登记的意义在于:简化注册流程、避免重复评审,同时有利于保证医疗器械的安全有效性。本文为大家说说医疗器械主文档登记流程:
截止2024年2月,我国已有387项医疗器械原材料或关键部件完成医疗器械主文档登记,医疗器械主文档内容主要涉及医疗器械的原材料和某些关键部件,而不是成品的医疗器械。我国推动医疗器械主文档登记的意义在于:简化注册流程、避免重复评审,同时有利于保证医疗器械的安全有效性。本文为大家说说医疗器械主文档登记流程:
医疗器械主文档登记流程
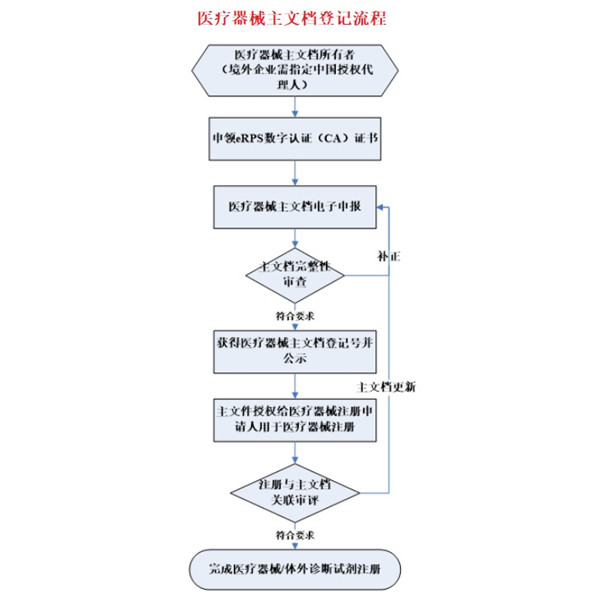
主文档登记资料及签章等内容适用于医疗器械注册电子申报相关要求。主文档所有者或其代理机构申领eRPS系统配套使用的数字认证证书(Certificate Authority,CA)后,在电子申报系统中提交医疗器械主文档登记申请表或医疗器械主文档登记更新申请表、申请表随附登记资料、技术资料等登记资料。资料提交成功后,器审中心向主文档所有者或其代理机构发送医疗器械主文档登记回执。登记回执仅证明主文档存档待查,供医疗器械产品注册等申报事项引用。国家药监局器审中心将适时在其官方网站公开主文档登记相关信息,以便于公众查询。
如有医疗器械主文档登记办理服务需求,欢迎您随时方便与杭州证标客医药技术咨询有限公司联络,联系人:叶工,电话:18058734169,微信同。