2023年国家医疗器械抽检复检工作要求
一、当事人对检验结论有异议的,自收到检验结论之日起(不含当日)7个工作日内,向医疗器械注册人备案人或者进口产品代理人所在地省级药品监督管理部门提出复检申请(以下简称受理复检申请的省级药品监督管理部门)。对同一检验报告的复检申请只办理一次。逾期、重复提出复检申请的不予受理。
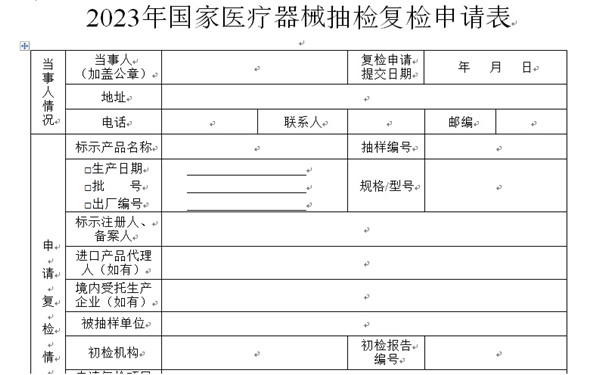
当事人应当填写《2023年国家医疗器械抽检复检申请表》(附录1,以下简称《复检申请表》),并提交《2023年国家医疗器械抽检结果送达告知书》(附录2,以下简称《送达告知书》)复印件等在《医疗器械质量抽查检验管理办法》(以下简称《办法》)第三十三条中所规定的资料。
二、受理复检申请的省级药品监督管理部门收到《复检申请表》时,应当依照《办法》及2023年国家医疗器械抽查检验方案相关规定,决定是否接受复检申请,并依据2023年国家医疗器械抽检复检机构名单确定复检机构,复检机构不得拒绝。受理复检申请的省级药品监督管理部门做出复检决定后,当事人不可撤销复检申请。
受理复检申请的省级药品监督管理部门应当自收到《复检申请表》之日起(不含当日)5个工作日内,登录国家医疗器械抽检信息系统(以下简称国家抽检系统),填写《2023年国家医疗器械抽检复检通知书》(附录3,以下简称《通知书》),打印并加盖做出复检决定的部门公章,在做出复检决定当日内交付给当事人,同时告知其复检机构联系方式,通知其主动联系复检机构办理复检相关事宜。
三、当事人应当自收到《通知书》之日起(不含当日)5个工作日内向复检机构预先支付复检费用。逾期未交的,复检机构有权取消复检并通知受理复检申请的省级药品监督管理部门。因未支付复检费用而取消复检的,对该批初检报告不得再次申请复检。若申请,受理复检申请的省级药品监督管理部门应当拒绝,并在《通知书》中说明原因。
四、复检机构应当自收到复检费用之日起(不含当日)3个工作日内向初检机构发出调样通知。
五、初检机构应当自收到调样通知起(不含当日)5个工作日内向复检机构发送样品,并向其复函告知复检报告传递要求。样品运输费用由初检机构承担。
六、检验过程沟通、复检费用支付、复检样品退还、复检报告传递、复检信息录入等工作要求依照现行《办法》《国家医疗器械质量抽查检验工作程序》相关规定执行。