在医疗机构中使用,与本公司生产的一次性使用磁定 位心脏脉冲电场消融导管配合使用,用于 治疗药物难治性、复发性、症状性的阵发性房颤的心脏脉冲电场消融系统,在我国属于第三类医疗器械注册产品,且不在免于开展医疗器械临床试验目录之内,本文为大家带来心脏脉冲电场消融系统临床试验设计实例,一起看正文。
在医疗机构中使用,与本公司生产的一次性使用磁定
位心脏脉冲电场消融导管配合使用,用于
治疗药物难治性、复发性、症状性的阵发性房颤的心脏脉冲电场消融系统,在我国属于第三类医疗器械注册产品,且不在免于开展医疗器械临床试验目录之内,本文为大家带来心脏脉冲电场消融系统临床试验设计实例,一起看正文。
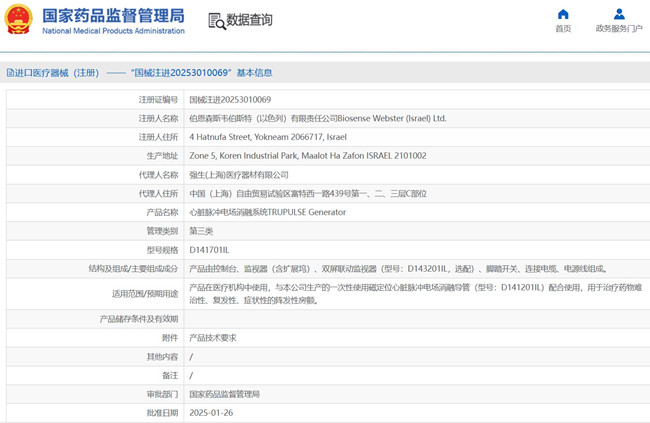
心脏脉冲电场消融系统临床试验设计实例
医疗器械临床试验的目的为评价产
品的安全有效性。临床试验包括探索性研究和确证性研究,其
中确证性临床试验的设计为前瞻性、非随机、多中心、单组目标值设计,计划入组 248 例受试者。
主要有效性评价指标为:在有效性评价期间(术后第 91-365
天),心电图数据(心电图(ECG),电话传输远程心电图(TTM)或
动态心电图(Holter))未记录到持续≥30 秒的(有症状和无症
状)快速房性心律失常(房颤、房速或不明原因的房扑)发作。
并且无下面失败模式中的任何一种,包括:即刻手术失败,重复消融失败(空白期内大于 1 次重复消融,在有效性评价期内任何重复消融),非研究导管使用失败(使用非研究导管进行肺静脉补点和左房非肺静脉房颤靶点的治疗),抗心律失常药物
(AAD)失败(使用新的 I 类/III 类 AAD 治疗房颤、房速或不明原因的房扑,或服用更高剂量的既往治疗失败的 I 类/III 类
AAD),标准12导联ECG记录持续的房颤/房速/房扑,以及直流电心脏复律失败。
主要安全性指标为早发性(消融术后 7 天内)主要不良事件的发生,包括:死亡(器械相关或手术相关),心房食管瘘,
心包填塞/穿孔,心肌梗死,卒中/脑血管意外,血栓栓塞,短暂
性脑缺血发作,膈神经损伤/膈肌麻痹,心脏传导阻滞,肺静脉
狭窄,肺水肿(呼吸功能不全)迷走神经损伤/胃轻瘫,心包炎,
重大血管穿刺并发症/出血。其中,房颤消融术后 90 天内出现的心房食管瘘,房颤消融术后 30 天内出现心包填塞/穿孔,12 个月随访期间发生的肺静脉狭窄及永久性膈神经麻痹,消融手术
期间或术后任意时间发生的器械或手术相关死亡,均被视为主要不良事件。其他安全性终点包括:非预期器械不良反应(UADE)
等。
次要评价指标包括:(1) 生活质量改善:消融术后 12 个月房颤对生活质量评分的影响,评估生活质量较基线的改善;
(2)即刻手术成功,定义为手术结束时所有确认传入阻滞完成肺静脉电隔离的受试者百分比;(3)重复消融手术;(4)有效性评价期间(术后第 91 天-365 天)心电图数据(ECG 或 TTM
或 Holter)未记录到≥30 秒的(症状性和无症状)快速房性心
律失常发作,但符合以下标准的情况也被视为手术失败:在 3
个月随访访视窗后服用任何抗心律失常药物(I 类或 III 类)
治疗房颤;(5)12 个月单次手术治疗成功;(6)12 个月临床成
功;(7)降低心血管事件住院率:定义为与入组前 6 个月相比,
术后 12 个月因心血管事件住院率降低;(8)心脏直流电复律减
少率:定义为与入组前 6 个月相比,术后 12 个月心脏直流电复
律率降低;(9)手术数据,包括:总手术时间、PFA 有效放电
时间、标测时间和 PFA 放电次数、总 X 线透视时间、左心房研
究导管停留时间;(10)试验用器械使用。
确证性临床试验实际入组受试者 277 例,安全性分析集患者 277 例,改良意向治疗分析集 mITT 274 例,符合方案分析集
PPS 255 例,在符合方案分析集的患者中,药物难治性症状性复
发性阵发性房颤患者 203 例。在符合方案分析集的 255 例受试
者中,12 个月成功率为 74.4%,精确单侧 97.5%置信下限为
68.5%,大于预先规定的性能目标。结果表明该研究符合主要有
效性成功标准。
符合方案分析集 255 例受试者显示(1)生活质量持续显著
改善与基线相比,12 个月时生活质量(AFEQT)评分平均变化
为 32.033 分;(2)使用研究导管进行消融的所有受试者(100%)
均实现了肺静脉传入阻滞,获得即刻手术成功;(3)在符合方
案分析集中,少数受试者(9%:23/255)在有效评价期内接受
了重复消融;(4)消融后 12 个月未记录到房颤/房速/房扑发作
且停用 AAD 治疗的受试者比例为 70.6%;(5)记录到症状性复
发的 12 个月单次手术治疗成功率为 88.2%;(6)消融后 12 个
月临床成功的受试者比例为 94.7%;(7)与基线相比,术后 12
个月时因心血管事件住院率降低 100%。术后 12 个月的加拿大
心血管学会-房颤的严重程度(CCS-SAF)评分相对基线的平均
变化为-2.60,表明生活质量改善。(8)与基线相比,12 个月时
直流电复律发生率降低 90.7%;(9)在 277 例导管插入受试者
中,平均总手术时间(±标准差)为 95.14±37.19 分钟,平均 PFA有效放电时间为 17.96±4.67 秒。平均标测时间为 7.67±5.03 分钟,
平均 PFA 有效放电次数为 74.1± 19.29 次,平均总 X 线透视时间
为 9.99±12.20 min,平均左心房研究导管停留时间为 43.83±18.19
分钟;(10)所有受试者都使用试验用器械消融了肺静脉靶点。
在 mITT 分析集的 274 名受试者中,未发生器械或手术相关死
亡、心房食道瘘、心肌梗死、血栓栓塞、膈神经损伤/膈肌麻痹、
心脏传导阻滞、肺静脉狭窄、肺水肿和迷走神经损伤/胃轻瘫。
试验中主要不良事件发生率为 2.9%,精确单侧 97.5%置信区间
上限为 5.7%,低于预先规定的12%性能目标。共有 8 名受试者报告了 9 例主要不良事件,心包填塞/穿孔(3)、重大血管穿刺
并发症/出血(2)、心包炎(1)、卒中/脑血管意外(2)和短暂性脑缺血发作(1)。所有受试者在随访结束前均达到已恢复/已缓解。未发生非预期器械不良反应。
如有医疗器械临床试验设计服务需求,欢迎您随时方便与杭州证标客医药技术咨询有限公司联络,联系人:叶工,电话:18058734169,微信同。